2023年8月8日, 诺和诺德公布了司美格鲁肽注射剂历时5年、1.7万人的三期试验结果(SELECT临床),结果显示,与安慰剂相比,每周一次皮下注射2.4 mg司美格鲁肽可使无糖尿病史的超重或肥胖成人发生重大不良心血管事件的风险降低20%,证明了GLP-1在减重和控糖以外更多的市场潜力。此结果的公布,使得诺和诺德股票大涨17%,市值突破4200亿美元。
司美格鲁肽是一种胰高血糖素样肽-1(GLP-1)受体激动剂,先后于2017年9月和2021年6月获批用于治疗2型糖尿病患者的血糖控制和肥胖患者的减重。诺和诺德预计于今年在美国和欧盟申请司美格鲁肽扩展标签适应症的监管批准,届时司美格鲁肽将成为首个通过减肥预防心血管疾病的药物。
GLP-1受体激动剂药物开发历程
胰高血糖素样肽-1(GLP-1)是一种由人胰高血糖素基因编码、肠道L细胞分泌的肽类激素,属于肠促胰岛素家族,GLP-1在人体内以GLP-1(7-36)和GLP-1(7-37)两种活性形式存在, 人体内主要以含30个氨基酸的GLP-1(7-36)为主,其次为31个氨基酸的GLP-1(7-37)。GLP-1具有促进胰岛素分泌、抑制胰高血糖素分泌、延迟胃排空等作用,因其独特的作用机制成为了2型糖尿病的重要靶标。天然的GLP-1因半衰期短(人类静脉给药1.5分钟,皮下给药1.5小时),释放后被二肽基肽酶 IV(DPP-4)快速分解而失去促胰岛素分泌活性,达不到治疗的效果。为使 GLP-1 更好地应用于临床,需对其结构进行修饰,在保留其与GLP-1受体结合并发挥生物学效应的同时使其不易被DPP-4快速降解,从而延长半衰期,增加活性GLP-1水平以达到药理浓度,这类药物即 GLP-1 受体激动剂。
自2005年首个GLP-1受体激动剂药物Exenatide(艾塞那肽)获批,目前已有多款GLP-1药物获批上市,见表1。艾塞那肽是一款合成的GLP-1类似物,最初在美国毒蜥的毒液中被发现,其半衰期仅2.4小时,需要一天注射两次。为了减少用药频率,阿斯利康开发了艾塞那肽长效缓释注射悬液,用药频次降低为一周一次。Liraglutide(利拉鲁肽)是诺和诺德开发的一种GLP-1类似物,与天然GLP-1有97%的同源性,通过将GLP-1主肽链修饰脂肪酸链,来增加药物与白蛋白的亲和力,成功将药物的半衰期延长到13小时,注射频率变为一天一次。Semaglutide(司美格鲁肽)是诺和诺德开发的利拉鲁肽“二代药”,经过进一步的结构改造提高了药物对白蛋白的亲和力及对DPP-4降解的抵抗力,药物的半衰期延长到一周,实现了一周给药一次。

表1 目前获批的GLP-1受体激动剂药物
司美格鲁肽片开发历程和挑战
经过科研人员的不断努力,GLP-1受体激动剂药物的半衰期被逐渐延长,剂型也从最开始的一天两次的短效注射,变为一周一次的长效注射剂。尽管注射频率在降低,对于需要长期用药的糖尿病患者,更为方便的口服治疗方式仍是未被满足的需求。然而,多肽口服使用,存在易被消化酶以及胃酸分解而失活,胃肠道黏膜穿透能力差,口服生物利用度极低等问题,使得开发GLP-1受体激动剂药物口服剂型存在巨大的挑战。
为了解决上述挑战,理想的多肽需要具有较大的治疗指数(Therapeutic Index),在胃肠道中有一定的稳定性、较长的半衰期以及较低的清除率。多肽的口服给药技术在许多文献中有所报导,包括渗透增强剂、纳米颗粒、肠道微装置、基于脂质的药物递送系统或疏水离子配对等。其中,渗透增强剂与纳米技术、基于装置的系统相比,更容易应用到制剂中,故而被广泛研究。
N- (8-(2-羟基苯甲酰)氨基)辛酸钠,简称SNAC,是由Emisphere公司在20世纪90年代开发的,从众多促渗透剂中筛选出来的高效载体分子。它是一种合成的两性水杨酸的N-乙酰化氨基酸衍生物,可作为载体的渗透增强剂。2014年,口服维生素B12(氰钴胺/SNAC)的批准,首次证明了SNAC是可行且安全的。随后,SNAC作为低渗透性药物的增渗剂被广泛的研究。
2017年,司美格鲁肽注射剂在美国获批,用于治疗2型糖尿病,随后新增了减重适应症。司美格鲁肽由于其长半衰期(皮下给药后约7天)和更加高效成为SNAC口服给药较理想的候选药物。司美格鲁肽结构如图所示,其肽主链是由酵母发酵产生的,26号位赖氨酸使用亲水性间隔剂和C18脂肪二酸修饰,以增加与白蛋白的亲和力,避免药物被肾脏快速清除,延长药物半衰期。8号位丙氨酸被α-氨基异丁酸取代,以抵抗DPP-4的降解。34号位使用了精氨酸取代赖氨酸,以确保只能连接一条脂肪二酸侧链,提高侧链的稳定性。
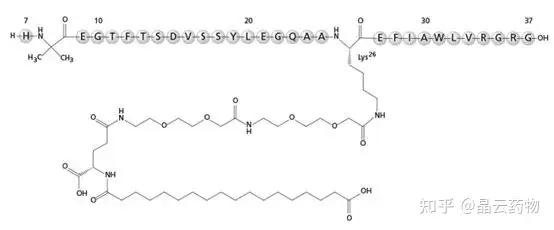
图1 司美格鲁肽结构图
诺和诺德开发的司美格鲁肽口服片使用SNAC作为渗透促进剂,SNAC在口服司美格鲁肽中可能的作用机理如图1所示。当片剂在胃内崩解后时,SNAC通过缓冲作用导致胃内局部pH升高,胃pH值的升高可减少胃蛋白酶降解司美格鲁肽。另一方面,SNAC通过改变溶解片剂的溶液极性来促进司美格鲁肽的单体化,从而削弱疏水相互作用。司美格鲁肽的吸收增强主要来源于SNAC的间接作用,SNAC结合到胃细胞的脂质膜中,使得胃上皮细胞膜流化(固体到流体的结构转变),进而允许司美格鲁肽跨细胞通过,研究发现,司美格鲁肽的吸收主要发生在胃部。
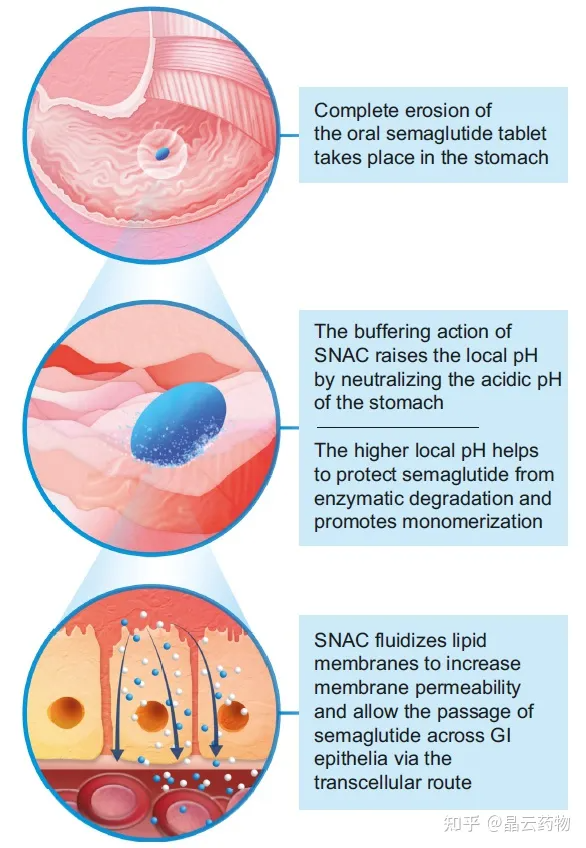
图 2 司美格鲁肽分子的吸收和保护机制
司美格鲁肽片产品介绍
诺和诺德的司美格鲁肽片(商品名Rybelsus®),是首款也是目前唯一一款上市的口服GLP-1受体激动剂药物,针对2型糖尿病患者,患者可以在每日口服一粒司美格鲁肽片和每周注射一次司美格鲁肽间转换。司美格鲁肽片剂的成功获批标志着多肽药物给药领域的一个重要里程碑,为多肽药物治疗提供了一种便捷和患者友好的注射替代方案。
司美格鲁肽片,获批3 mg、7 mg、14 mg三种规格,自2019年9月在美国首批后,目前已在欧洲、日本、加拿大等多个国家获批销售,国内Rybelsus®已于2022年5月提交上市申请。Rybelsus®目前仅获批了2型糖尿病适应症,基于其更好的用药便利性,2022年Rybelsus®全球销售额已达16亿美元。此外,原研诺和诺德也正在开发司美格鲁肽50 mg片剂,并计划今年在美国和欧盟提交上市申请。2023年5月公布的Phase 3a OASIS试验显示,口服司美格鲁肽50 mg片剂与安慰剂相比,对于坚持治疗68周的患者,司美格鲁肽组的体重减轻17.4%,而安慰剂组的体重减轻1.8%,显示出优异的减重效果。
作为晶云药物的CDMO事业部,晶云星空聚焦于为小分子化药及多肽药物提供口服制剂的研发和生产服务,我们的核心技术团队具有丰富的口服制剂开发经验,包括难溶化合物,多肽类难渗药物等。我们相信,依托晶云药物强大的晶型和制剂研发技术平台,我们可以为您在司美格鲁肽片剂或者其他GLP-1受体激动剂药物的口服片剂开发上,提供坚实的技术支持。
总结和展望
GLP-1受体激动剂药物因具有优异的降糖效果、心血管保护作用及较好的减肥效果,尤其是在减肥领域巨大的市场潜力,成为了国内外许多药企争相布局的赛道,GLP-1受体激动剂药物作为代谢性疾病治疗药物,正在从降糖、减肥等治疗领域,向心血管、慢性肾病、非酒精性脂肪肝、阿尔茨海默症等高发领域拓展,如有新适应症的研发成功,未来更是前景无量。司美格鲁肽口服片剂的上市,为GLP-1受体激动剂药物的治疗提供了一种更加便捷和友好的用药方案,对多肽药物口服制剂的研发具有里程碑意义。
参考资料
[1] FDA官网
[2] 诺和诺德新闻:
[3] Manoj Kumar Mahapatra et al. Semaglutide, a glucagon like peptide‑1 receptor agonist with cardiovascular benefits for management of type 2 diabetes[J]. Reviews in Endocrine and Metabolic Disorders, 2022, 23:521–539.
[4] Vanita R. Aroda et al. A new era for oral peptides: SNAC and the development of oral semaglutide for the treatment of type 2 diabetes[J]. Reviews in Endocrine and Metabolic Disorders, 2022, 23:979–994.
[5] Andrew L. Lewis et al. Development and approval of rybelsus (oral semaglutide): ushering in a new era in peptide delivery[J]. Drug Delivery and Translational Research, 2022, 12:1-6.